
В
иноделие
и
иноградарство
2/2008
22
виноделие
Сорбция ионов металллов
из водных растворов и виноматериалов
хитинсодержащим комплексом
Е.Ю. ЕЛДИНОВА, О. Л. КИСЕЛЕВА, Г. Г. НЯНИКОВА, Т. Э. МАМЕТНАБИЕВ
Санкт-Петербургский государственный технологический институт (Технический университет)
ведение.
Хитин-глюкановый комп-
лекс (ХГК) является основным струк-
турообразующим компонентом кле-
точной стенки грибов. Хитин выполняет
также защитную функцию, предохраняя
клетки грибов от проникновения токсинов
[1]. Известно, что ХГК обладает выражен-
ными сорбционными свойствами в отно-
шении тяжелых металлов и радионуклидов
[2–4].
Повысить сорбционную активность
ХГК можно путем дезацетилирования.
Образующийся при этом хитозан-глю-
кановый комплекс (ХЗГК) имеет боль-
ший по сравнению с ХГК сорбционный
потенциал за счет увеличения числа
реакционноспособных аминогрупп, обра-
зующих комплексы с ионами металлов
по механизму хелатообразования. При
этом сорбирующая способность ХЗГК кор-
релирует с уровнем дезацетилирования
(
Л. А. Нудьга, С. И. Ганичева, В. А. Петрова,
Е. А. Быстрова, Е. Б. Львова, А. В. Галкин,
Г. А. Петропавловский
, 1997).
В настоящее время в винодельческой
промышленности все еще существует
проблема предупреждения металличе-
ских помутнений виноматериалов и вин,
вызванных присутствием избыточного
количества ионов металлов, в основном
железа. Используемые традиционно деме-
таллизаторы имеют ряд серьезных недо-
статков (токсичность, многостадийность
обработки, возможность возникновения
повторных помутнений), что приводит
к необходимости поиска нового препа-
рата. ХЗГК обладает комплексом ценных
свойств, позволяющих рекомендовать его
в качестве деметаллизатора вин.
Цель данной работы
— исследование
характеристик хитин- и хитозан-глюкано-
вого комплексов, полученных из мицелия
Aspergillus niger
, и изучение возможности
использования их для снижения избыточ-
ного количества металлов в виноматериа-
лах.
Объекты и методы исследования.
Исходным материалом служил мице-
лий гриба
Aspergillus niger
штамм ТИ-12,
являющийся продуцентом лимонной кис-
лоты, из коллекции кафедры технологии
микробиологического синтеза СПбГТИ
(ТУ). Гриб выращивали глубинным спосо-
бом на мелассно-солевой среде в колбах
на качалке с перемешиванием в режиме
220 об/мин при 28 °С в течение 7 сут.
Выход биомассы определяли весовым
методом, концентрацию титруемых кис-
лот в культуральной жидкости — прямым
титрованием гидроксидом натрия в при-
сутствии фенолфталеина [5].
Мицелий отделяли от жидкой фазы
фильтрованием на нутч-фильтре.
С целью выделения из мицелия ХГК
проводили деминерализацию (обработка
10%-ным раствором HCl в течение 2 ч),
депротеинирование 2,5%-ным раствором
NaOH в течение 24 ч. Для получения ХЗГК
хитин-глюкановый комплекс подвергли
деацетилированию 40%-ным раствором
NaOH при 130 °С в течение 2 ч).
В
В полученных образцах хитин- и хито-
зан-глюкановых комплексов определяли
влажность весовым методом. Элементный
анализ образцов сорбентов проводили
методом электронно-зондового микро-
анализа с использованием рентгеновского
микроанализатора энергодисперсионного
Link-860.
Поглотительную способность по воде и
бензолу определяли эксикаторным мето-
дом (
Г. И Бойкова, М. Я. Пулеревич
, 1983),
площадь удельной поверхности — методом
тепловой десорбции азота (
Л.Н. Ворожбитова,
Г.К. Ивахнюк, С.Д. Колосенцев, А.Г. Черепов
,
1991), полную статическую емкость мате-
риалов — по стандартной методике (ГОСТ
20255.1–89
«Иониты. Методы определения
статической ионообменной емкости»
).
Сорбционную емкость рассчитывали
по формуле
СЕ
Fe
3+
= (
СЕ
исх
Fe
3+
–
СЕ
равн
Fe
3+
)/
К
,
где
СЕ
исх
Fe
3+
— исходная концентрация
ионов Fe
3+
, мг/дм;
СЕ
равн
Fe
3+
— равновесная
концентрация ионов Fe
3+
, мг/дм;
К
— кон-
центрация сорбента, г/дм.
Для изучения сорбции ионов метал-
лов из виноматериалов навеску сорбен-
та (0,25 г/дм
3
) вносили в виноматериал,
перемешивали на качалке со скоростью
150 об/мин при комнатной температуре
в течение 2 ч. Концентрацию ионов желе-
за (III) в виноматериале создавали с помо-
щью FeCl
3
· 6H
2
O. Содержание металлов
в виноматериалах до и после обработки
сорбентами определяли стандартизован-
ным химическим методом с окончанием
на ICP / Эшелле-спектрометре модели
PC1000 (Leeman Labs. Inc., USA), снабжен-
ном источником высокочастотной индук-
тивно-связанной плазмы.
Результаты и их обсуждение.
Через
7 сут культивирования
Aspergillus niger
на мелассно-солевой среде количество
биомассы составило 18 г/дм
3
, содержание
Показатель
Хитин-глюкановый комплекс
грибной
Хитин
крабовый
Удельная поверхность, м
2
/г
0,80
0,20
Поглотительная способность, см
3
/г:
по воде
0,27
0,14
по бензолу
0,10
0,01
Полная сорбционная обменная емкость по Na
+
:
мг-экв/г
0,0366
3,24
мг/г
1,13
74,5
Таблица 1
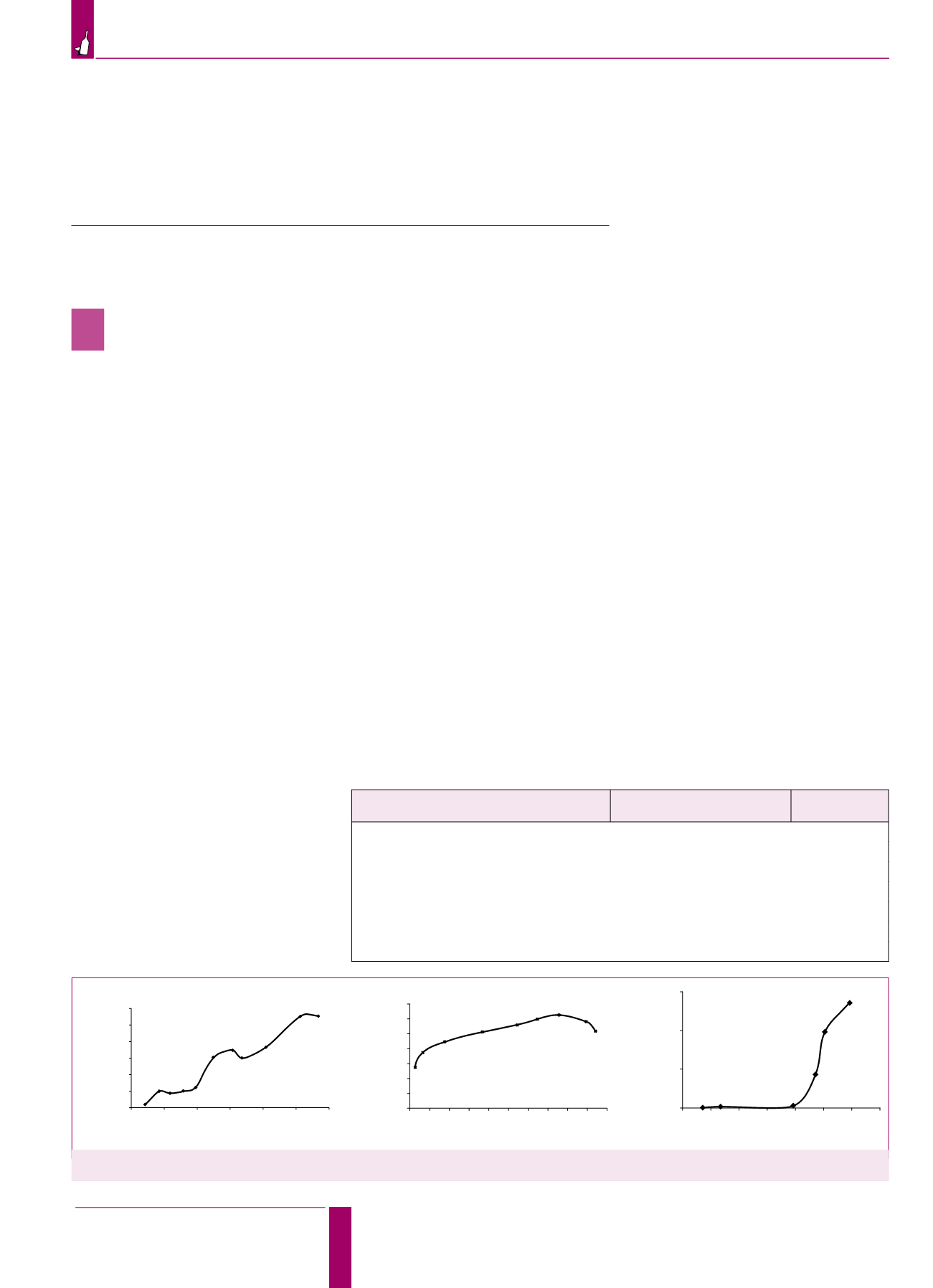
Рис. 1.
Изотерма сорбции Cu
2+
(
а
), Pb
2+
(
б
) и Ni
2+
(
в
) хитин-глюкановым комплексом
600
500
400
300
200
100
0
Статическая сорбционная
емкость, мг/г
Равновесная концентрация Cu
2+
, г/дм
3
а
350
300
250
200
150
100
50
0
Статическая сорбционная
емкость, мг/г
Равновесная концентрация Pb
2+
, г/дм
3
б
450
300
150
0
Статическая сорбционная
емкость, мг/г
Равновесная концентрация Ni
2+
, г/дм
3
0
1
2
3
4
5
6
7
в
0 2 4 6 8 10 12
0 2 4 6 8 10 12 14 16 18 20
Электронная Научная СельскоХозяйственная Библи т ка









