
67
ПИЩЕВАЯ ПРОМЫШЛЕННОСТЬ
12/2010
FOOD PROVISION SECURITY
QUALITY AND SAFETY FOODSTAFFS
жуток времени из реакционной сре
ды отбирали пробы, нейтрализовали
до величины рН 6, фильтровали и
определяли их углеводный состав на
жидкостном хроматографе. На рис. 1
показано изменение углеводного со
става в реакционной среде при гид
ролизе лабораторного образца ЦД.
При увеличении продолжительности
гидролиза количество циклодекст
рина в реакционной смеси снижает
ся (кривая 1).
На хроматограммах наблюдается
появление нового соединения, име
ющего молекулярную массу больше,
чем исходный ЦД (кривая 2). Оче
видно, что ЦД в кислой среде обра
зует комплексы, состоящие из не
скольких молекул ЦД и проявляю
щиеся раньше при хроматографи
ческом разделении. Максимальное
количество таких комплексов обра
зовалось через 45 мин после начала
процесса гидролиза. В дальнейшем
эти комплексы также подвергаются
гидролизу, их количество снижается.
Однако при увеличении продолжи
тельности процесса количество этих
комплексов стабилизируется и со
ставляет около 20 % от всех углево
дов, находящихся в реакционной
среде. Остальная часть ЦД подверга
ется кислотному гидролизу с образо
ванием глюкозы, мальтозы и триса
харов.
Таким образом, водный раствор
ЦД под воздействием кислоты при
температуре 95
0
С гидролизуется до
простых сахаров (около 70 % от ис
ходного количества) и образует ус
тойчивые комплексы, состоящие из
двух или больше циклодекстрино
вых колец.
В дальнейшем исследовали фер
ментативный гидролиз ЦД. Для гид
ролиза использовали глюкоамилаз
ный ферментный препарат типа
AMG E производства компании
Novozymes (Дания) с активностью
300 AГЕ/мл (амилоглюкозидазных
единиц) [5]. Изучали гидролиз трех
образцов ЦД – лабораторного,
представляющего смесь разных
форм ЦД, и двух промышленных –
α
ЦД и
β
ЦД. Гидролиз водных ра
створов ЦД концентрацией 5 % про
водили при температуре 60
0
С и ве
личине рН 4,8. В каждом из трех
опытов исследовали процесс гидро
лиза двух одинаковых образцов ра
створа ЦД с различной дозировкой
ферментного препарата – 400 AГЕ/кг
и 2000 AГЕ/кг на 1 кг сухого веще
ства ЦД.
На рис. 2 приведено изменение уг
леводного состава при гидролизе
лабораторного образца ЦД.
При дозировке глюкоамилазы 400
AГЕ/кг сухих веществ исходного ЦД
соединение гидролизуется незначи
тельно, всего около 10 % за 22 ч гид
ролиза. Указанная дозировка фер
ментного препарата обычно приме
няется при проведении гидролиза
крахмала до глюкозы, причем за это
время гидролизуется обычно около
90 % крахмала [6]. При повышении
дозировки фермента до 2000 AГЕ/кг
процесс гидролиза значительно ус
коряется и за 22 ч ЦД гидролизуется
наполовину. Характерная неожидан
ная особенность гидролиза ЦД со
стоит в том, что гидролиз протекает
сразу до глюкозы без образования
других сахаров – мальтозы, трисаха
ров и др.
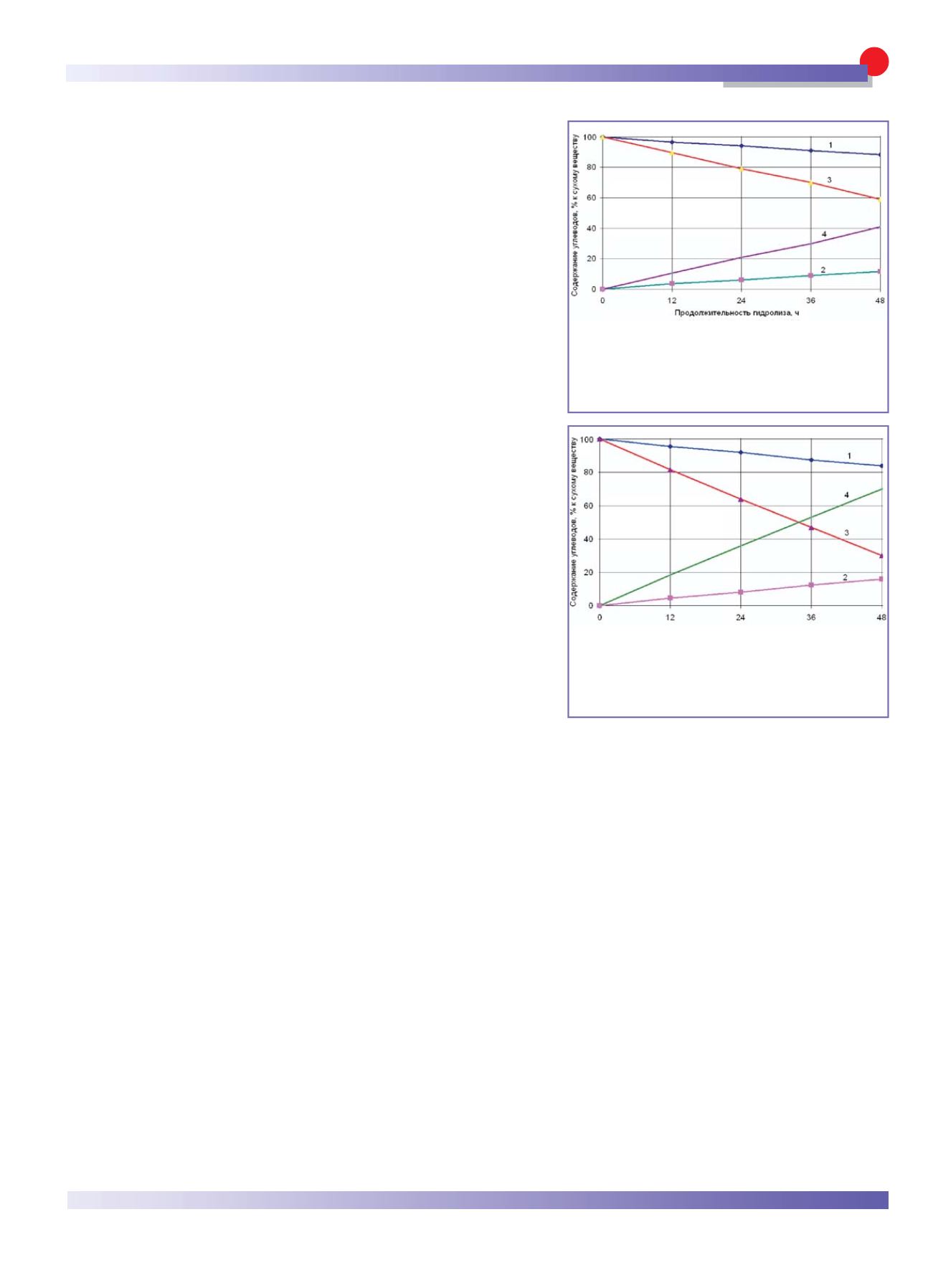
На рис. 3 приведены результаты
хроматографического определения
углеводного состава в реакционной
среде при ферментативном гидро
лизе образца
α
–ЦД в водном ра
створе, а на рис. 4 – образца
β
–ЦД.
Как видно из графиков,
α
ЦД зна
чительно устойчивее к гидролити
ческому воздействию фермента глю
коамилазы, чем
β
–ЦД, скорость гид
ролиза которого почти в два раза
выше. Половина количества
α
–ЦД
гидролизуется за 60 ч, а
β
–ЦД – за
30 ч. Однако во всех случаях гидро
лиз ЦД протекает сразу до глюкозы
без заметного образования проме
жуточных продуктов гидролиза. Это
можно объяснить особым механиз
мом воздействия фермента на коль
цеобразное соединение ЦД, кото
рый заслуживает отдельного глубо
кого изучения.
Таким образом, проведенные ис
следования показывают, что при
организации промышленного произ
водства ЦД для гидролиза крах
мальных остатков кислотный гидро
лиз использовать нецелесообразно.
Ферментативный гидролиз при уме
ренной дозировке глюкоамилазы
позволяет избавиться от высокомо
лекулярных углеводных примесей
Рис. 3. Изменение углеводного состава при
ферментативном гидролизе
α
ЦД: дозировка
глюкоамилазы – 400 AGU/кг: 1 – циклодекстрин;
2 – глюкоза; дозировка глюкоамилазы – 2000 AGU/кг;
3 – циклодекстрин; 4 – глюкоза
без значительного снижения выхода
ЦД.
ЛИТЕРАТУРА
1.
Szejtl, J.
Cyclodextrin Tehnology/
J.
Szejtl
.– Kluver, 1984.
2.
Абелян, В.А.
Циклодекстрины:
Получение и применение/В.А. Абе
лян. – Ереван: Изд. Дом «Ван Арь
ян», 2001. – 519 с.
3.
Hydrolysis
of Cyclodextrin by
Aspergillus oryzae Amylase/
I. Jodal [et
al.]
//Starch Starke.– 1984.– V.19.–
№ 4.– P.P. 140–143.
4.
ГОСТ Р
51985–2002 «Крахмал
кукурузный. Общие технические ус
ловия». – М.: Изд во стандартов,
2002.
5.
Проспекты
компании «Novozy
mes» (Дания).
6.
Крахмал
и крахмалопродукты/
Н.Г. Гулюк и др. – М.: Агропромиз
дат, 1985.
Рис. 4. Изменение углеводного состава при
ферментативном гидролизе
β
ЦД: дозировка
глюкоамилазы – 400 AGU/кг: 1 – циклодекстрин;
2 – глюкоза; дозировка глюкоамилазы – 2000 AGU/кг;
3 – циклодекстрин; 4 – глюкоза
Э ектронная Научная СельскоХозяйственная Библиотека









