
Молочнохозяйственный вестник, №4 (16), IV кв. 2014
65
ТЕХНИЧЕСКИЕ НАУКИ
воды обладают моносахара, затем дисахариды и полисахариды, что согласуется с
литературными данными [7].
Активность воды согласно теории Ван-Лаара [8,9]:
Tk
xU
e х
а
⋅
⋅
⋅ − =
2
0
) 1(
1
, (1)
где (1-х) - мольная доля воды;
х – мольная доля сахарозаменителя;
U0 – энергия взаимообмена (среднее увеличение энергии одной молекулы при
замене ее соседних молекул другими), Дж;
k - постоянная Больцмана, Дж/К;
Т- температура, К.
Коэффициент активности воды составит:
,
2
0
1
Tk
xU
e
⋅
⋅
=
γ
(2)
После логарифмирования из уравнения (2) было получено:
Tk
xU
⋅
⋅
=
2
0
1
ln
γ
. (3)
По экспериментальным данным по активности воды (рисунок 1) был рассчи-
тан коэффициент активности, а затем из уравнения (3) были определены значения
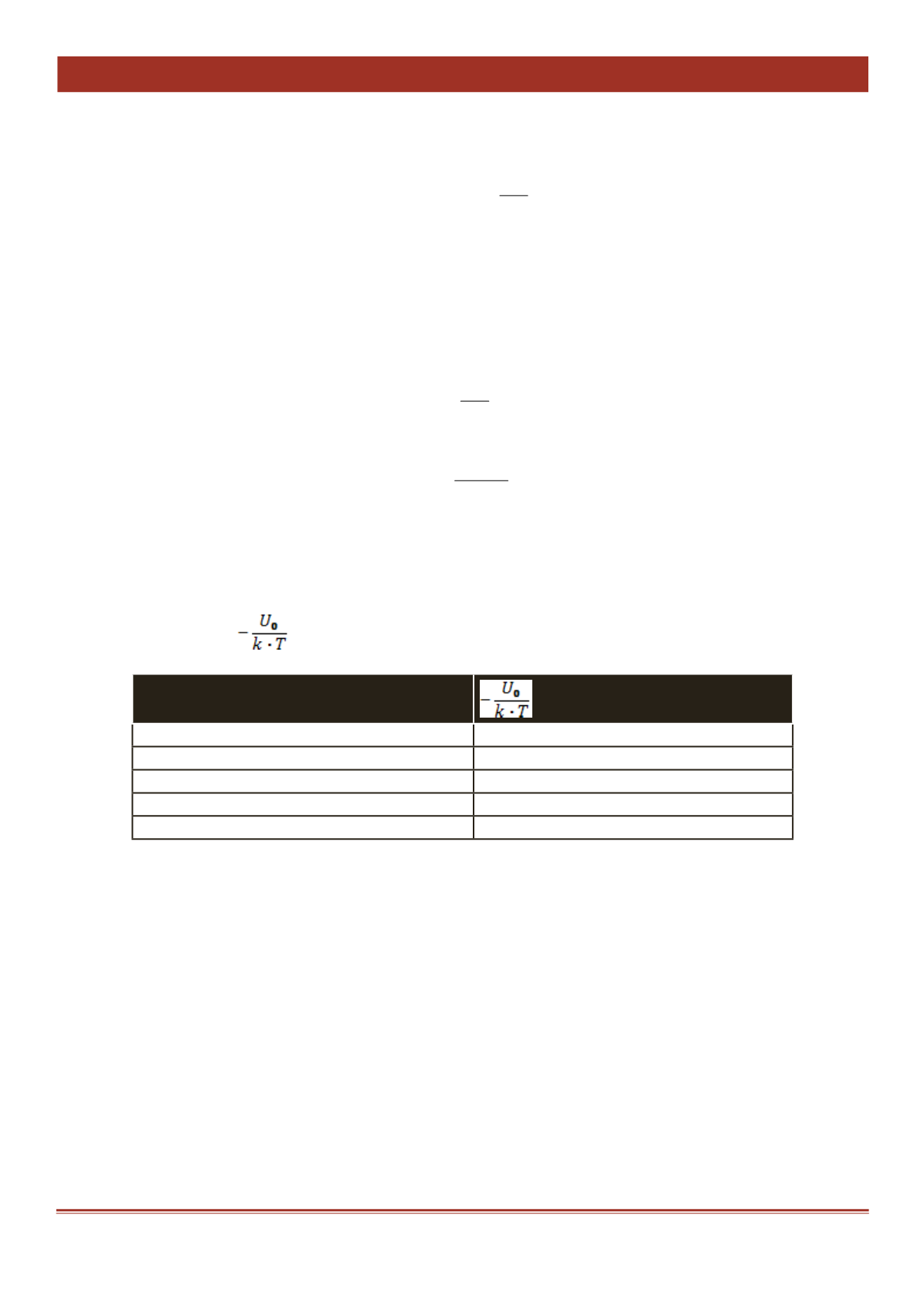
-U0/(к Т) и представлены в таблице 1.
Таблица 1 –
Значения
для водных растворов сахаров
Наименование углевода
Фруктоза
1,95
Глюкоза
2,76
Сахароза
5,11
Мальтоза
7,86
Мальтодекстрин
78,31
Из рисунка 1 и данных таблицы 1 следует, что чем выше активность воды
в растворах и чем большее значение -U0/ (к•Т) имеет вещество, тем ниже кон-
сервирующий эффект этого вещества. Следовательно, значение -U0/(к•Т) может
быть использовано для оценки консервирующей способности, которая возрастает
в ряду: мальтодекстрин, мальтоза, сахароза, глюкоза, фруктоза.
Затем по уравнению (2) с учетом найденных значений -U0/(к Т) был рассчи-
тан коэффициент активности воды и его значение сравнено с экспериментальным
данными. Относительная погрешность отклонений расчетных значений от экспери-
ментальных составила в среднем 7,92 %, что свидетельствует о том, что представ-
ленные выше теоретические уравнения могут быть применены для вычисления
активности и коэффициента активности воды в растворах изученных углеводов.
Для бинарного раствора для состояния равновесия связь между коэффици-
ентами активности воды γ
1
и растворенного вещества γ
2
может быть установлена
согласно [8, 9] в виде уравнения:
Электронная Научная СельскоХозяйственная Библиотека









