
03.06.2017 Разработка биотехнологического приема и отбора по признаку высокой, генетически детерминированной устойчивости организма к стрессу
http://aeconomy.ru/science/agro/razrabotkabiotekhnologicheskogopr/4/9
(лейкоцитов) проводили в тонкой части мазка, где эритроциты лежат одиночно. Для
нахождения процента разрушенных мононуклеаров крови животного под действием 0,2%
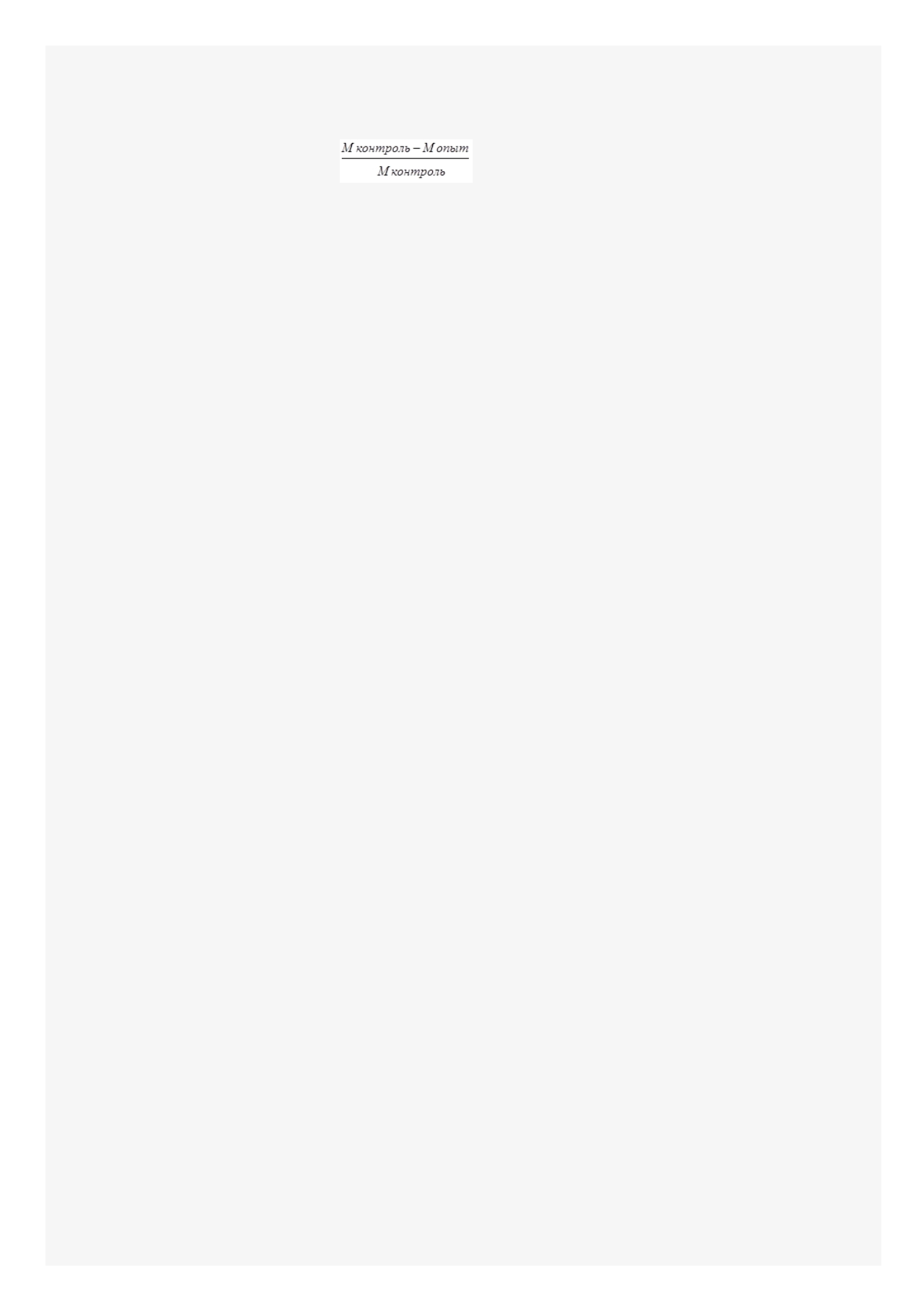
раствора норадреналина гидротартрата использовали формулу:
ПСРМ =
· 100;
Где ПСРМ – показатель стрессрезистентности мононуклеаров; М – мононуклеары.
Состояние естественной резистентности оценивалось по показателям опсонофагоцитарной
реакции (В.С. Гостев, 1951); лизоцимной активности сыворотки крови (В.Г. Дорофейчук,
1963); титру гетерогемагглютининов.
Для определения стрессреакции брали кровь и выявляли состояние стресса в аппарате
Панченкова. Затем в пипетку набирали 0,1% раствор адреналина гидрохлорида, доведенный
до изотонической концентрации хлористым натрием, до метки Р и выливали на часовое стекло.
После этого пипетку прополаскивали раствором гепарина до метки Р и той же пипеткой
набирали кровь у животного до метки К и выливали на часовое стекло в раствор адреналина
гидрохлорида. Кровь и раствор адреналина гидрохлорида перемешивали концом пипетки и
наполняли эту же пипетку адреналиногидрохлоридной кровью до метки О и ставили в штатив.
Аналогичным образом ставили контрольные пробы с изотоническим раствором хлористого
натрия содержащий 0,01 н. раствор соляной кислоты. Исходя из того, что раствор адреналина
гидрохлорида содержит 0,01 н. раствор соляной кислоты, в контрольную пробу добавляли
0,01 н. раствор соляной кислоты. РН 0,1% раствора адреналина гидрохлорида и
изотонического раствора хлористого натрия после добавления 0,01 н. раствора соляной
кислоты имели одинаковые величины.
Результаты стрессреакции организма животных в опытных и контрольных пробах определяли
по скорости оседания эритроцитов через 15 минут. Учет осуществляли визуально. Состояние
стресса констатировали в том случае, когда разница скорости оседания эритроцитов в опытной
и контрольной пробах составляла 0,3 мм и выше. Стрессреакции с определением скорости
оседания эритроцитов периферической крови в 0,1% растворе адреналина гидрохлорида в
аппарате Т.Н. Панченкова за 15 минут.
Биохимические методы применяли при определении белковой картины крови. Общий белок
определяли рефрактометрически; а белковые фракции – электрофорезом в теле агара
(П.Грабар, П. Буртен, 1963). Количество общего кальция в сыворотке комплексонометрически.
Неорганический фосфор в сыворотке крови – по Бриггсу в модификации С.И. Ивановского
/1972/. Резервную щелочность в плазме крови – по ВанСляйку (1969).
Гематологические методы применялись для определения количества эритроцитов, лейкоцитов,
гемоглобина, скорости оседания эритроцитов, бляшкообразующих
клеток и
розеткообразующих лейкоцитов крови. Содержание эритроцитов и концентрацию гемоглобина
определяли фотоэлектроколометрическим методом (Г.В. Дервиз, А.И. Воробьева, 1959).
Лейкоциты подсчитывали в счетной камере, скорость оседания эритроцитов – в аппарате Т.Н.
Панченкова. Количество аутоиммунных бляшкообразующих клеток определяли по методике
Н.Н. Клемнарской (1978). Аутоиммунные розеткообразующие клетки в мазках крови
животных, окрашенных по РомановскомуГимза, обнаруживали путем подсчета 100 клеток в
двух продольных полосках мазка. Дифференциальный подсчет лейкоцитов проводился в
мазках, окрашенных по методу РомановскогоГимза.
В качестве показателей уровня морфофункционального развития новорожденных животных
использовали живую массу, размеры, тип телосложения, проявления врожденных рефлексов,
клинические показатели (частота пульса и дыхания). Об интенсивности роста и развития
молодняка жвачных животных судили по абсолютному приросту и среднесуточному приросту.
В качестве объекта исследования и определения стрессчувствительности новорожденных
животных использовали периферическую кровь из пуповины и яремной вены.
Для определения стрессчувствительности в две пробирки вносили по 0,1 мл крови
новорожденного животного. В первую пробирку (опытную) добавляли 0,9 мл 0,1% раствора
адреналина гидрохлорида, а во вторую (контрольную) 0,9 мл. стерильного физиологического
раствора. Пробы тщательно перемешивали и ставили в термостат на 30, 60, 120 минут при
температуре 37,5˚ С. После инкубирования через 30, 60, 120 минут перед каждым очередным
подсчетом брали 0,1 мл. взвеси с опытной и контрольной проб и смешивали с 0,1 мл. 1%
раствором водного метилрозацилина или метилвиолета той же концентрации и объема. Затем
содержимым обеих проб заполняли камеру Горяева и подсчитывали количество лейкоцитов в
25 больших квадратах по обычной методике, принятой для подсчетов. Для нахождения
процента разрушенных лейкоцитов новорожденного животного под воздействием 0,1%
раствора адреналина гидрохлорида использовали формулу:
Электронная Научная СельскоХозяйственная Библиотека









